CAPA-Software
Das von der GMP und zahlreichen ISO/FDA Regelwerken wie ISO 13485 und FDA 21 CFR 820 geforderte Konzept der Corrective and Preventive Actions ist eine Schlüsselmethode des Qualitätsmanagements in der Medizintechnik. Mit einer abteilungsübergreifenden Softwarelösung wie CAQ.Net können Sie CAPAs nicht nur effektiv durchführen, sondern verfügen über ein global einsetzbares Werkzeug, mit dem Sie das gesamte Qualitätswesen überwachen, steuern und dokumentieren können. Hierfür stellt CAQ.Net verschiedene Techniken für unterschiedliche Facetten des Qualitätswesens bereit, welches es in einer modularen Software vereint.
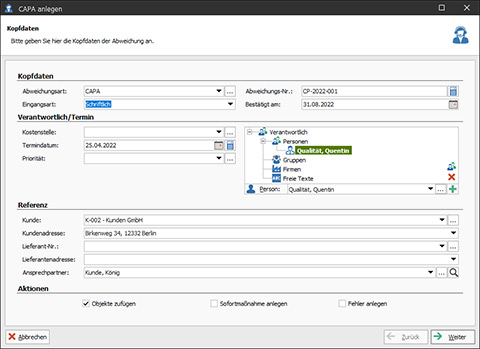 CAPA-Assistent in der CAQ.Net Software
CAPA-Assistent in der CAQ.Net Software
Corrective and Preventive Actions
Mit dem CAPA-Konzept können Sie mögliche Ursachen für aufgetretene Qualitätsmängel ergründen, diese anschließend lösen und Arbeitsabläufe, Produkte oder Herstellungsverfahren anpassen, um eine Wiederkehr des Mangels zu verhindern. Hierbei sollte der gesamte Produktionsprozess von der Lieferantenauswahl und der Wareneingangsprüfung über die Qualitätsprüfung bis hin zur Reklamationsbearbeitung einsehbar sein und die notwendigen Daten jederzeit zur Verfügung stehen.
Warum eine CAPA-Software?
Wenn aber die Unversehrtheit eingegangener Waren, die Qualitätsprüfung und das Reklamationsmanagement händisch dokumentiert werden oder in separaten Excel-Dateien gepflegt werden, fehlen bereits zwei Schlüsselfähigkeiten, um einen effektiven CAPA-Prozess durchführen zu können: Informationstransparenz und Datenkompatibilität. Um ebendies zu ermöglichen und einen vollständigen PDCA-Kreislauf aufrechtzuhalten kommt CAQ.Net ganz im Sinne einer CAPA-Software zum Einsatz.
CAPA in CAQ.Net
Die CAQ.Net Software besteht aus sämtlichen Bausteinen die notwendig sind, um die Qualität eines Produkts vom Entstehungsprozess bis zum Reklamationsmanagement, über den gesamten Produktlebenszyklus hinaus, zu überwachen und zu dokumentieren. Somit können Sie im Falle einer CAPA mit nur einem System auf sämtliche qualitätsrelevante Daten eines Produkts zugreifen und mittels einer Fehler-Ursachen-Analyse die tatsächlichen Grundursachen eines Qualitätsmangels identifizieren. Ob vom Zulieferer bezogenes Rohmaterial, ein fehlerhafter Produktionsschritt oder mangelhaft geschultes Personal die Ursache (Root Cause) für den Qualitätsmangel ist, können Sie also anhand nur eines Systems ergründen.
Assistentengestützte CAPA-Software
Da der Grund für die Auslösung einer CAPA in den verschiedensten Bereichen des Qualitätswesens auftreten kann, ist in CAQ.Net der CAPA-Prozess nicht in Form eines eigenständigen Software-Moduls umgesetzt, sondern als modulübergreifende, assistentengestützte Funktion im gesamten System verfügbar. Wenn der Auslöser beispielsweise im Prüfmittelmanagement, in der Schulungsverwaltung, im Auditmanagement, oder in der Reklamationsbearbeitung liegt, können Sie direkt im entsprechenden Modul von CAQ.Net den CAPA-Prozess anhand weniger Schritte im Assistenten einleiten.
Mit CAPA-Software CAPAs vermeiden
CAQ.Net ist ein global einsetzbares Werkzeug, mit dem das gesamte Qualitätswesen überwacht, gesteuert und dokumentiert werden kann, damit die Gründe für eine mögliche CAPA im Vorhinein bereits innerhalb des Produktentstehungsprozesses so gut wie möglich ausgeschlossen werden können. Denn, entgegen weitverbreiteter Meinung, stellt der CAPA-Prozess im Sinne der FDA vielmehr die Ultima Ratio im Qualitätsmanagement dar und sollte nicht übermäßig eingeleitet werden.